引言:2020年12月18日���,藥監總局發(fā)布2項醫療器械注冊答疑����,詳見(jiàn)正文��。
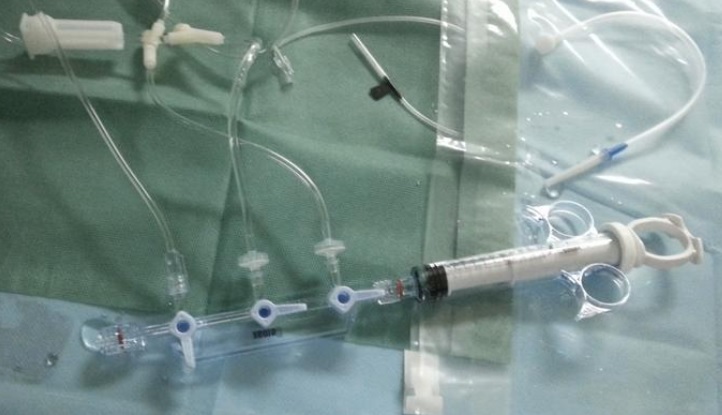
一����、對血管內造影導管的動(dòng)力注射要求有哪些:
1)對于采用高壓注射裝置注射的造影導管產(chǎn)品��,需在技術(shù)要求和說(shuō)明書(shū)(標簽)中標注最大爆破壓力信息��,同時(shí)按照YY0285.1-2017對動(dòng)力注射要求進(jìn)行規定����。
2)對于采用環(huán)柄注射器注射造影劑的造影導管產(chǎn)品�,可不制定動(dòng)力注射要求����。宜在說(shuō)明書(shū)中明確以下警示:請勿使用高壓注射裝置注射造影劑��。
適用范圍中包含血管造影功能的其他導管��,宜參照以上要求�����。
二����、體外診斷設備說(shuō)明書(shū)發(fā)生變化該怎么辦:
根據《醫療器械說(shuō)明書(shū)和標簽管理規定》(6號令)第十六條規定:“已注冊的醫療器械發(fā)生注冊變更的�����,申請人應當在取得變更文件后����,依據變更文件自行修改說(shuō)明書(shū)和標簽�。說(shuō)明書(shū)的其他內容發(fā)生變化的����,應當向醫療器械注冊的審批部門(mén)書(shū)面告知��,并提交說(shuō)明書(shū)更改情況對比說(shuō)明等相關(guān)文件�?!?/span>