2024年2月5日��,國家藥監局發(fā)布《2023年度醫療器械注冊工作報告》��,為大家介紹了2023年全年我國醫療器械注冊總體情況����,一起看正文����。
2024年2月5日�,國家藥監局發(fā)布《2023年度醫療器械注冊工作報告》��,為大家介紹了2023年全年我國醫療器械注冊總體情況���,一起看正文��。
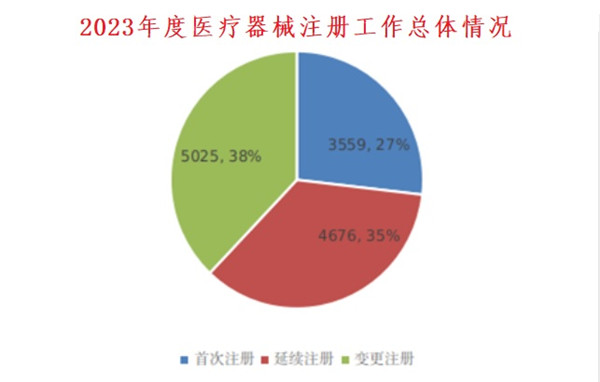
2023年度醫療器械注冊總體情況
(一)醫療器械監管法規制度體系更加完善��。2023年9月8日����,十四屆全國人大常委會(huì )將《醫療器械管理法》列入立法規劃項目��,國家藥監局已成立工作領(lǐng)導小組�、工作組���、專(zhuān)家咨詢(xún)組�,著(zhù)手起草相關(guān)法律文本���。會(huì )同國家衛生健康委���、國家疾控局聯(lián)合印發(fā)《醫療器械緊急使用管理規定(試行)》�����,為醫療器械緊急使用提供法律支撐��。起草《醫療機構臨床急需醫療器械臨時(shí)進(jìn)口使用管理要求》���。
(二)創(chuàng )新醫療器械質(zhì)量數量實(shí)現雙豐收���。2023年�����,國家藥監局共批準創(chuàng )新醫療器械61個(gè)����,優(yōu)先審批醫療器械12個(gè)��,創(chuàng )新醫療器械批準數量再創(chuàng )新高�����,比2022年增加6個(gè)�。在數量增加的同時(shí)����,創(chuàng )新醫療器械“含金量”不斷提升��,在全球率先批準通過(guò)破壞交感神經(jīng)治療肺動(dòng)脈高壓的一次性使用環(huán)形肺動(dòng)脈射頻消融導管上市��,單光子發(fā)射及X射線(xiàn)計算機斷層成像系統�、腹腔內窺鏡單孔手術(shù)系統��、顱內取栓支架等產(chǎn)品技術(shù)達到國際領(lǐng)先水平�����,更好地滿(mǎn)足了公眾使用高端醫療器械的需求�。
(三)服務(wù)國家重大戰略穩步實(shí)施��。大力支持京津冀�����、長(cháng)三角����、粵港澳大灣區�����、海南自貿港���、福建等重點(diǎn)區域建設���。批準人工耳蝸聲音處理器等3個(gè)海南臨床真實(shí)世界應用試點(diǎn)產(chǎn)品上市����,截至目前���,累計批準產(chǎn)品9個(gè)��,惠及更多患者��。指導召開(kāi)第二屆博鰲國際藥械真實(shí)世界研究大會(huì )��。指導粵港澳大灣區使用20種�����、29批次港澳已上市的醫療器械��,服務(wù)區域診療需要�����。設立醫療器械創(chuàng )新山東��、北京����、河北�����、湖北服務(wù)站����,創(chuàng )新服務(wù)站數量已達11個(gè)�����,服務(wù)區域產(chǎn)業(yè)高質(zhì)量發(fā)展成效初步顯現���。推進(jìn)人工智能醫療器械��、生物材料創(chuàng )新任務(wù)揭榜掛帥工作����,共遴選出48個(gè)人工智能醫療器械���、40個(gè)生物材料揭榜項目��?�;I建高端醫療裝備創(chuàng )新合作平臺���,加速高端醫療器械創(chuàng )新轉化速度����。完善前置申請機制��,加大前置審評輔導力度����,9個(gè)產(chǎn)品通過(guò)輔導已申請注冊��。
(四)常態(tài)化疫情防控保障有力����。應急批準廣東�、北京����、江蘇3家企業(yè)的3個(gè)國產(chǎn)體外膜肺氧合系統(ECMO)上市����,助力疫情防控“保健康��、防重癥”目標落實(shí)��。全年批準新冠病毒檢測試劑21個(gè)��,其中核酸檢測試劑9個(gè)�,抗原檢測試劑12個(gè)���。截至目前累計批準新冠病毒檢測試劑157個(gè)�,充分滿(mǎn)足疫情防控需要����。協(xié)同國家衛生健康委���、國家疾控局聯(lián)合推進(jìn)猴痘檢測試劑產(chǎn)品研發(fā)和產(chǎn)品注冊上市�。持續做好新冠病毒變異株監測和檢測試劑能力評估�����,確保產(chǎn)品有效檢出能力��。
(五)醫療器械注冊備案管理水平顯著(zhù)提升����。部署各地開(kāi)展第二類(lèi)醫療器械注冊清理規范全面整改���,召開(kāi)全國第二類(lèi)醫療器械注冊管理工作會(huì )議�����,印發(fā)強化醫療器械注冊管理工作意見(jiàn)���,部署全面加強注冊管理有關(guān)工作����。對一次性使用微波消融針���、重組膠原蛋白創(chuàng )面敷料等��,出臺相關(guān)文件和指導原則��,統一規范注冊工作要求��。指導基層做好第一類(lèi)醫療器械備案工作�����。持續規范第一類(lèi)產(chǎn)品備案���,切實(shí)加強對市級監管部門(mén)的監督指導�。
(六)醫療器械臨床試驗管理力度繼續加大�����。開(kāi)展27個(gè)品種的臨床試驗產(chǎn)品真實(shí)性核查�����,31個(gè)品種的臨床試驗監督抽查�,較2022年數量加倍����。發(fā)布監督抽查情況通報一期���,對存在問(wèn)題的產(chǎn)品嚴肅處理�,作出不予注冊��、一年內不予受理的決定���。截至2023年底�����,醫療器械臨床試驗機構備案數量達到1340家����,與2022年相比增加13.8%���。
(七)醫療器械標準質(zhì)量不斷提升����。修訂發(fā)布《醫療器械標準報批發(fā)布工作細則》《醫療器械標準驗證工作細則》��,制定《醫療器械標準實(shí)施評價(jià)工作細則》等文件����,標準制修訂管理更加精細��。成立全國醫用防護標準化工作組及口腔數字化醫療器械�����、醫療器械可靠性與維修性等2個(gè)標準化技術(shù)歸口單位����。發(fā)布28項醫療器械國家標準�����、131項行業(yè)標準及14項行業(yè)標準修改單�����。截至2022年底����,現行有效醫療器械標準共1974項���,其中國家標準271項���,行業(yè)標準1703項�,與國際標準一致性程度超過(guò)90%��,標準體系覆蓋性���、系統性不斷提升�。我國主導制定的ISO 24072《輸液器進(jìn)氣器件氣溶膠細菌截留試驗方法》國際標準正式發(fā)布����,2名中國專(zhuān)家當選國際電工組織(IEC)技術(shù)委員會(huì )副主席和分技術(shù)委員會(huì )主席�,《人工智能醫療器械 肺部影像輔助分析軟件 算法性能測試方法》標準獲批國際標準立項�。發(fā)布《國家藥品監督管理局關(guān)于GB 9706.1-2020及配套并列標準�����、專(zhuān)用標準實(shí)施有關(guān)工作的通告》及兩期解讀�����,印發(fā)《GB 9706.1-2020標準檢驗要點(diǎn)》�����,公開(kāi)發(fā)布41個(gè)新版GB 9706系列標準的檢驗報告模板�����,建立專(zhuān)家咨詢(xún)機制�,有效推動(dòng)新版GB 9706系列標準的平穩有序實(shí)施�����。
(八)醫療器械分類(lèi)管理扎實(shí)推進(jìn)�����。發(fā)布《關(guān)于進(jìn)一步加強和完善醫療器械分類(lèi)管理工作的意見(jiàn)》�,強化分類(lèi)管理頂層設計�����。完成醫療器械分類(lèi)技術(shù)委員會(huì )換屆工作�,修訂發(fā)布《醫療器械分類(lèi)技術(shù)委員會(huì )工作規則》��。動(dòng)態(tài)調整分類(lèi)目錄���,發(fā)布《關(guān)于調整〈醫療器械分類(lèi)目錄〉部分內容的公告》���,涉及58個(gè)產(chǎn)品����。發(fā)布《重組膠原蛋白生物材料命名指導原則》解讀�,進(jìn)一步指導和規范醫療器械領(lǐng)域重組膠原蛋白生物材料的命名����。組織成立中醫(民族醫)器械專(zhuān)項工作小組�����,統籌開(kāi)展中醫(民族醫)器械分類(lèi)�、命名���、標準�、審評��、檢驗����、核查等工作�����。
(九)醫療器械唯一標識工作有序開(kāi)展�。開(kāi)展唯一標識第一批���、第二批實(shí)施工作總結����,通報先進(jìn)經(jīng)驗做法�����。發(fā)布《關(guān)于做好第三批實(shí)施醫療器械唯一標識工作的公告》��,將臨床需求量較大的一次性使用產(chǎn)品�����、集中帶量采購中選產(chǎn)品�����、醫療美容相關(guān)產(chǎn)品等103種風(fēng)險較高的第二類(lèi)醫療器械納入第三批實(shí)施范圍���。組建醫療器械唯一標識專(zhuān)家咨詢(xún)團隊���,為深入推進(jìn)唯一標識實(shí)施工作提供支撐�。制定《醫療器械唯一標識的形式和內容》《醫療器械唯一標識的包裝實(shí)施和應用》兩項醫療器械行業(yè)標準��,進(jìn)一步指導醫療器械唯一標識工作實(shí)施����。
(十)監管科學(xué)研究工作成果顯著(zhù)���。組織推進(jìn)第二批監管科學(xué)6個(gè)重點(diǎn)項目13個(gè)醫療器械子項目工作��,已形成醫療器械監管新工具��、新標準��、新方法141項����。組織藥品監管科學(xué)體系建設第一批重點(diǎn)項目醫療器械領(lǐng)域重點(diǎn)項目申請和遴選���;啟動(dòng)新一代基因測序產(chǎn)品評價(jià)方法研究��、數字療法醫療器械質(zhì)量評價(jià)方法研究等9項重點(diǎn)項目����。配合開(kāi)展監管科學(xué)研究基地和重點(diǎn)實(shí)驗室考核�����,促進(jìn)研究質(zhì)量提升����。
(十一)醫療器械技術(shù)審查能力持續提升���。技術(shù)審評質(zhì)量管理體系與業(yè)務(wù)工作高效融合����,審評質(zhì)量監測�����、運行和改進(jìn)體系持續完善���。醫療器械注冊審評購買(mǎi)服務(wù)工作穩步實(shí)施�。長(cháng)三角�、大灣區審評分中心審評人員數量分別增加176%����、109%�����。全年發(fā)布67項指導原則和6項審評要點(diǎn)�,現行有效指導原則達到613項�����,對醫療器械分類(lèi)目錄覆蓋率達92.2%�。持續開(kāi)展全系統醫療器械注冊管理實(shí)務(wù)培訓���、充分發(fā)揮實(shí)訓基地作用����,線(xiàn)上舉行12期省級醫療器械審評審批人員線(xiàn)上培訓����,8300余人參訓����,舉辦首次省級醫療器械審評員線(xiàn)下實(shí)地培訓�����,提升培訓效果���。公開(kāi)已發(fā)布的GB 9706相關(guān)醫療器械標準解讀視頻����,150余萬(wàn)人次在線(xiàn)瀏覽學(xué)習���。