第二類(lèi)體外診斷試劑變更注冊常見(jiàn)發(fā)補問(wèn)題
發(fā)布日期:2023-06-13 19:37瀏覽次數:618次
寫(xiě)有關(guān)醫療器械變更注冊事項的文章比較多����,以為體外診斷試劑相對常規器械更加穩定�����,較少寫(xiě)有關(guān)體外診斷試劑變更注冊這個(gè)話(huà)題����。本文帶大家一起了解第二類(lèi)體外診斷試劑變更注冊常見(jiàn)發(fā)補問(wèn)題���。
寫(xiě)有關(guān)醫療器械變更注冊事項的文章比較多�����,以為體外診斷試劑相對常規器械更加穩定����,較少寫(xiě)有關(guān)體外診斷試劑變更注冊這個(gè)話(huà)題����。本文帶大家一起了解第二類(lèi)體外診斷試劑變更注冊常見(jiàn)發(fā)補問(wèn)題�����。
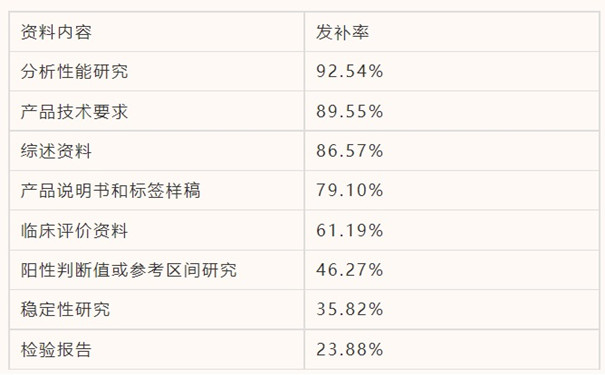
第二類(lèi)體外診斷試劑變更注冊常見(jiàn)發(fā)補問(wèn)題:
體外診斷試劑變更注冊最常見(jiàn)發(fā)補問(wèn)題是對變更內容的驗證和確認不夠充分���,或表述不規范���。大部分問(wèn)題與前文首次注冊常見(jiàn)問(wèn)題相同�����,不再贅述�����。另有一些注冊變更時(shí)需特別注意的問(wèn)題有:性能指標變更中�����,未提供變更指標在已獲批適用機型上的驗證資料��;未提供多批性能驗證資料��。檢驗方法變更中�,未提供相關(guān)驗證資料�����;未說(shuō)明變更方法的科學(xué)和理性��。參考區間變更中����,未對變更人群區間進(jìn)行說(shuō)明或驗證�����。產(chǎn)品技術(shù)要求變更中�����,變更申請項目描述不規范���;變更后的產(chǎn)品技術(shù)要求的性能指標和檢驗方法未體現符合國家標準品的要求����。適用儀器變更中���,未提供新增機型的注冊證信息�����。除此之外��,部分變更申報資料的風(fēng)險分析報告中未對變更內容進(jìn)行風(fēng)險分析���,不能從產(chǎn)品的預期用途和與安全性等方面��,分析并識別變更的情況對于產(chǎn)品風(fēng)險狀態(tài)的影響����;還有一些申報資料的變更內容未在關(guān)聯(lián)項目(如技術(shù)要求和說(shuō)明書(shū))中進(jìn)行同步修正���。