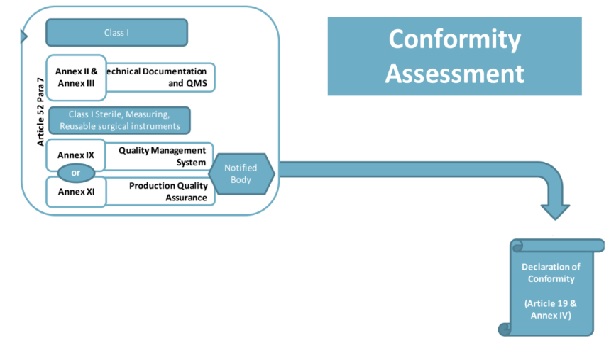
歐盟一類(lèi)醫療器械CE認證需要技術(shù)文件嗎
發(fā)布日期:2021-05-25 23:20瀏覽次數:2115次
明天是2021年5月26日���,是歐盟醫療器械法規MDR EU 2017/745因新冠疫情推遲一年后正式實(shí)施的日期����。對于一類(lèi)醫療器械��,很多客戶(hù)類(lèi)比成國內備案�����,認為非常簡(jiǎn)單����。從專(zhuān)業(yè)角度來(lái)看��,一類(lèi)醫療器械CE認證?與國內備案有先溝通之處����,但也存在較大差異�����。
引言:明天是2021年5月26日�����,是歐盟醫療器械法規MDR EU 2017/745因新冠疫情推遲一年后正式實(shí)施的日期���。對于一類(lèi)醫療器械�,很多客戶(hù)類(lèi)比成國內備案��,認為非常簡(jiǎn)單����。從專(zhuān)業(yè)角度來(lái)看���,一類(lèi)醫療器械CE認證與國內備案有先溝通之處�,但也存在較大差異��。
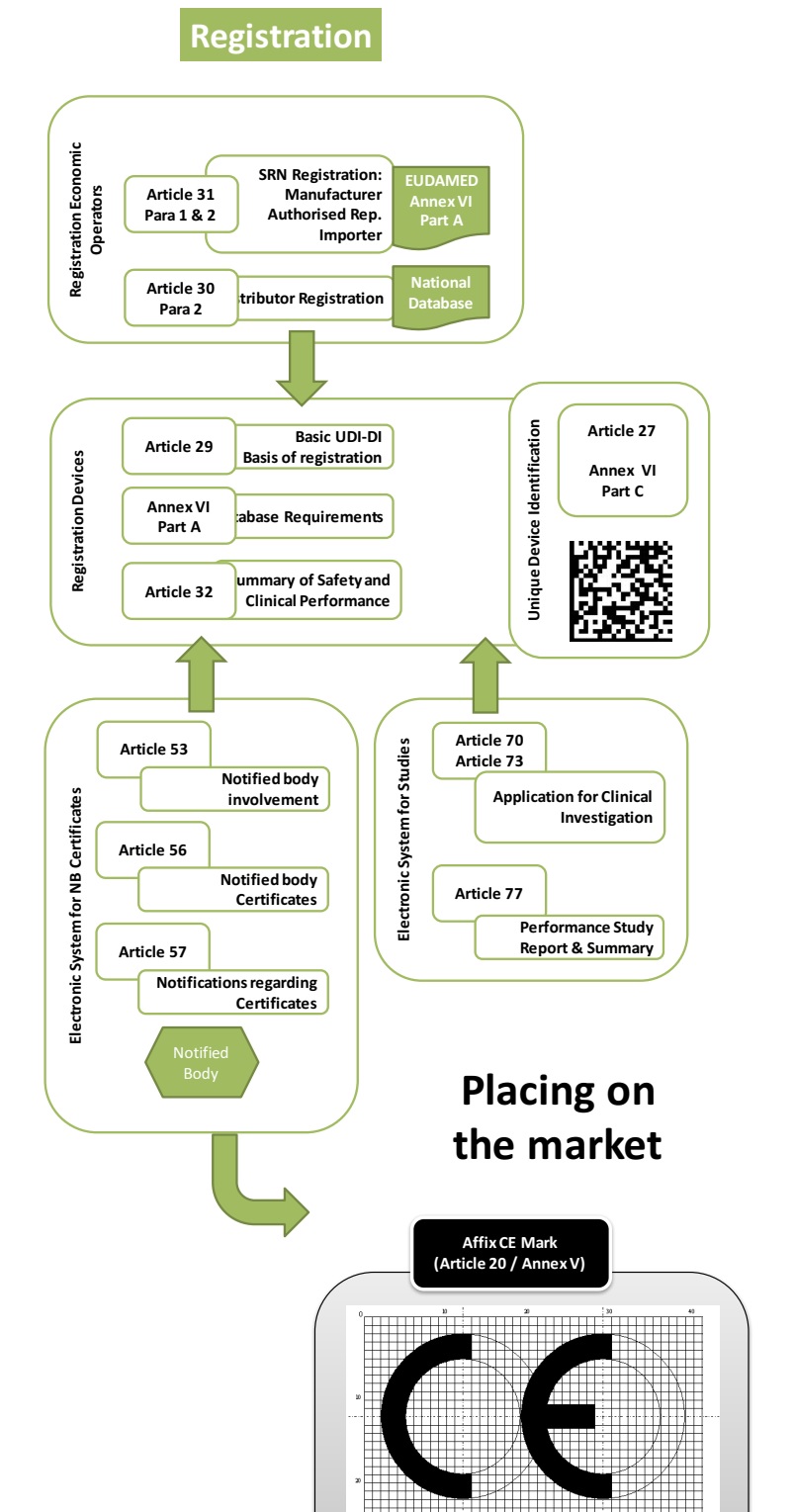
按照MDR的規定�,對于自我宣告類(lèi)器械�����,需要指定歐盟授權代表并完成器械注冊后�����,才可以合法加貼CE標志并上市銷(xiāo)售�。下圖是歐盟醫療器械注冊流程圖: