本文從醫療器械注冊檢驗���、注冊準備及注冊資料相關(guān)事項�,為朋友們講解醫用口罩注冊全程要點(diǎn)����?����?紤]到內容較多��,因此分成上下兩篇呈現�,方便讀者閱讀�����。
引言:本文從醫療器械注冊檢驗�、注冊準備及注冊資料相關(guān)事項�,為朋友們講解醫用口罩注冊全程要點(diǎn)��?��?紤]到內容較多���,因此分成上下兩篇呈現���,方便讀者閱讀���。
五���、醫用口罩的生產(chǎn)流程及主要設備
醫用口罩的生產(chǎn)流程見(jiàn)下圖: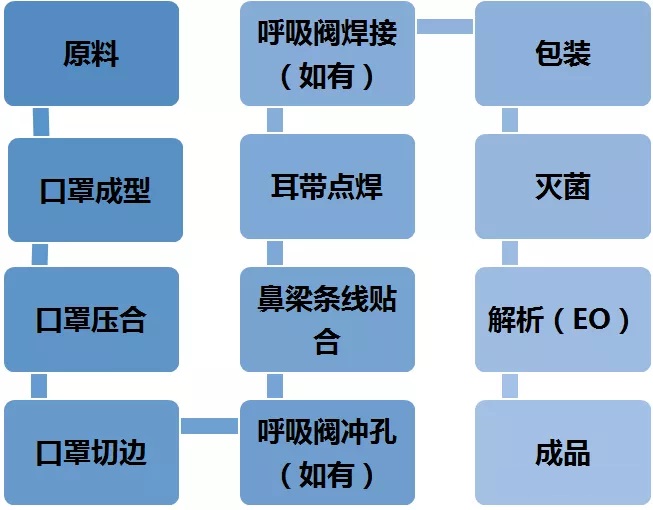
醫用口罩的主要生產(chǎn)設備如下:
六����、醫用口罩的滅菌
對于生產(chǎn)的醫用無(wú)菌口罩�,必須通過(guò)滅菌工序方可放行��。對于跨界進(jìn)行入口罩行業(yè)�����,這無(wú)疑是個(gè)門(mén)檻��。滅菌可以通過(guò)委托滅菌����,也可以購買(mǎi)滅菌設備自行滅菌�。市面上一般由環(huán)氧乙烷(EO)滅菌和輻照滅菌兩種方式����??紤]到輻照滅菌劑量控制不好會(huì )對熔噴布帶來(lái)影響導致過(guò)濾效率不符合要求�,所以絕大部分企業(yè)都選用EO滅菌����。由于EO滅菌使用的是有毒有害的環(huán)氧乙烷����,所以滅菌后還需進(jìn)行解析����,分為自然解析和滅菌柜解析�����。一般而言��,自然解析的周期約為14天��,才能確?��?谡种袣埩舻沫h(huán)氧乙烷達標����。
七�、醫用口罩的檢測要求
醫用口罩產(chǎn)品的檢測包括出廠(chǎng)檢驗和型式檢驗�。
出廠(chǎng)檢驗項目至少應有以下項目:外觀(guān)���、結構與尺寸��、鼻夾���、口罩帶����、微生物指標����、環(huán)氧乙烷殘留量(若采用環(huán)氧乙烷滅菌)的要求�。
型式檢驗應為產(chǎn)品標準的全性能檢驗�。

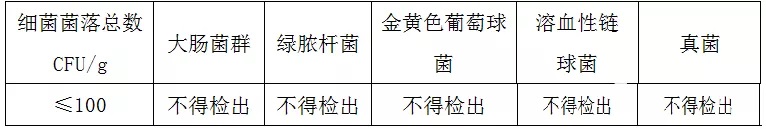
微生物指標��,滅菌口罩經(jīng)環(huán)氧乙烷滅菌����,應無(wú)菌����,其環(huán)氧乙烷的殘留量應不超過(guò) 10μg/g���。對于非滅菌口罩(普通級)應符合下表的要求�����。
八�����、醫用口罩存在的主要風(fēng)險
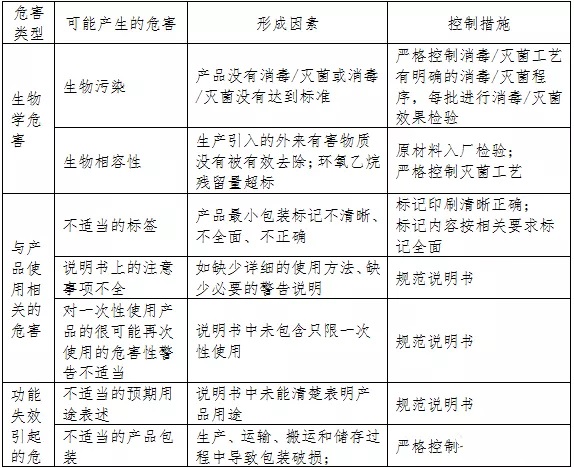
醫用口罩產(chǎn)品在進(jìn)行風(fēng)險分析時(shí)應符合YY/T0316-2008《醫療器械 風(fēng)險管理對醫療器械的應用》的要求�����。企業(yè)在進(jìn)行風(fēng)險分析時(shí)���,至少應考慮表中的主要危害�,企業(yè)還應根據自身產(chǎn)品特點(diǎn)確定其他危害��。針對產(chǎn)品的各項風(fēng)險����,企業(yè)應采取應對措施�����,確保風(fēng)險降到可接受的程度�����。
九�����、醫用口罩其他相關(guān)問(wèn)題
1���、鑒于目前對醫用口罩的過(guò)濾材料質(zhì)量難以通過(guò)便捷有效的檢驗方式來(lái)控制����,生產(chǎn)質(zhì)量管理體系的規范運行是企業(yè)保證口罩產(chǎn)品質(zhì)量穩定的主要手段����,故在醫療器械注冊技術(shù)審評和體系考核中審核員和檢查員會(huì )關(guān)注過(guò)濾材料的生產(chǎn)工藝及供貨來(lái)源��。企業(yè)應對產(chǎn)品的過(guò)濾材料進(jìn)行控制���,明確過(guò)濾材料的來(lái)源及質(zhì)量要求���,具有相對穩定的生產(chǎn)工藝及供貨來(lái)源以保證產(chǎn)品的質(zhì)量�����。
2�、醫用口罩是二類(lèi)醫療器械���,理應走注冊程序����。在疫情條件下����,部分省份可以進(jìn)行備案管理����,如廣東省明確對于在一級響應期間新增擬開(kāi)展醫用口罩���、防護服等屬于二類(lèi)防控器械產(chǎn)品注冊和生產(chǎn)的����,憑工信部門(mén)意見(jiàn)向所在地市藥監局申請備案�����,市局在備案憑證中應注明“本備案僅在公共衛生事件一級響應期間適用”���。備案后����,按以下方法放行:按照《中國藥典》(2015年版)第三部1101無(wú)菌檢測法開(kāi)展無(wú)菌檢驗�,在培養七天后未發(fā)現有微生物生長(cháng)���,其他理化指標均檢測合格��,可先放行���。產(chǎn)品標簽上應按照正常無(wú)菌檢測完成時(shí)間標注使用的起始時(shí)間���。企業(yè)在無(wú)菌檢驗后續培養觀(guān)察時(shí)間內�����,發(fā)現不符合要求的����,應及時(shí)召回�。
3�、醫用口罩的安全性�����、有效性只是其起到防護作用的一部分因素�?�?谡终_的使用及佩戴方法也直接影響了防護的效果�����。因此在說(shuō)明書(shū)中應明示出使用者需要的全部信息以避免口罩的誤用�����,降低交叉感染的風(fēng)險���。如注明佩戴方法�����、明確標識口罩正反面識別方法�����、使用時(shí)間的建議���、注明濾料級別或相關(guān)說(shuō)明等����。另外����,醫護人員對于不同種類(lèi)醫用口罩的適用范圍還沒(méi)有十分明確的認識���,應在說(shuō)明書(shū)中清楚地注明口罩的適用范圍并加強醫護人員的培訓工作�。
4��、無(wú)菌醫用口罩在10萬(wàn)級潔凈廠(chǎng)房條件下生產(chǎn)����,其特點(diǎn)是塵粒最大允許數大或等于0.5微米的粒子數不得超過(guò)3500000個(gè)�,大于或等于5微米的粒子數不得超過(guò)20000個(gè)�����。另外�����,微生物最大允許數��,浮游菌數不得超過(guò)500個(gè)每立方米�����;沉降菌數不得超過(guò)10個(gè)每培養皿�����。同時(shí)相同潔凈度等級的潔凈室壓差保持一致�,對于不同潔凈等級的相鄰潔凈室之間壓差要≥5Pa��,潔凈室與非潔凈室之間要≥10Pa��。這主要是為了保障空氣從潔凈區流向非潔凈區�,避免氣流倒灌��。溫度一般控制在冬季20——22℃�����;夏季24——26℃����;波動(dòng)±2℃���。冬季潔凈室濕度控制在30-50%����,夏季潔凈室濕度控制在50-70%�����。對溫度��、濕度無(wú)特殊要求時(shí)�,以穿著(zhù)潔凈工作服不產(chǎn)生舒服感為宜�。其功能布置�����、設備設施和管理要求可參考《醫療器械潔凈室(區)檢查要點(diǎn)指南》�。