2019年5月31日���,國家藥品監督管理局發(fā)布了《關(guān)于實(shí)施醫療器械注冊電子申報的公告》(2019年第46號)�,這標志著(zhù)eRPS系統建設工作的竣工�,也意味著(zhù)醫療器械注冊工作步入電子時(shí)代�����。
2019年5月31日�����,國家藥品監督管理局發(fā)布了《關(guān)于實(shí)施醫療器械注冊電子申報的公告》(2019年第46號)����,這標志著(zhù)eRPS系統建設工作的竣工�����,也意味著(zhù)醫療器械注冊工作步入電子時(shí)代����。
自2019年6月24日起��,eRPS系統正式開(kāi)通��,徹夜排隊遞交資料的現象將永遠成為歷史�����。國家藥品監督管理局醫療器械技術(shù)審評中心啟動(dòng)醫療器械eRPS將近一個(gè)月�,醫療器械注冊人面臨著(zhù)哪些困惑���?eRPS適用于幾類(lèi)器械�����?過(guò)渡期的注冊申報怎么辦�?境外企業(yè)的公證性文件拆分掃描后是否還具有效應����?諸多實(shí)操亟待解決��。

Q1:eRPS適用于幾類(lèi)器械�?
A:eRPS系統目前適用于境內三類(lèi)器械及進(jìn)口二三類(lèi)醫療器械及體外診斷試劑的注冊申請及臨床試驗審批�。
醫療器械注冊電子申報事項(共27項)列表
項目 | 子項 | 分項 | 受理流向 |
境內醫療器械注冊申請 | 境內醫療器械首次注冊 | 1.境內第三類(lèi)醫療器械注冊申請 | 國家器審中心 |
2.境內第三類(lèi)體外診斷試劑注冊申請 |
境內醫療器械變更申請 | 3.境內第三類(lèi)醫療器械注冊登記事項變更申請 |
4.境內第三類(lèi)醫療器械注冊許可事項變更申請 |
5.境內第三類(lèi)體外診斷試劑注冊登記事項變更申請 |
6.境內第三類(lèi)體外診斷試劑注冊許可事項變更申請 |
境內第三類(lèi)醫療器械延續注冊 | 7.境內第三類(lèi)醫療器械延續注冊申請 |
8.境內第三類(lèi)體外診斷試劑延續注冊申請 |
9.境內第三類(lèi)高風(fēng)險醫療器械臨床試驗審批申請 |
進(jìn)口醫療器械注冊申請 | 進(jìn)口醫療器械首次注冊申請 | 10.進(jìn)口第二��、三類(lèi)醫療器械注冊申請 | 國家器審中心 |
11.進(jìn)口第二類(lèi)體外診斷試劑注冊申請 |
12.進(jìn)口第三類(lèi)體外診斷試劑注冊申請 |
進(jìn)口醫療器械變更申請 | 13.進(jìn)口第二��、三類(lèi)醫療器械注冊登記事項變更申請 |
14.進(jìn)口第二�����、三類(lèi)醫療器械注冊許可事項變更申請 |
15.進(jìn)口第二�、三類(lèi)體外診斷試劑注冊登記事項變更申請 |
16.進(jìn)口第二�����、三類(lèi)體外診斷試劑注冊許可事項變更申請 |
進(jìn)口醫療器械延續注冊 | 17.進(jìn)口第二�、三類(lèi)醫療器械延續注冊申請 |
18.進(jìn)口第二��、三類(lèi)體外診斷試劑延續注冊申請 |
19.進(jìn)口第三類(lèi)高風(fēng)險醫療器械臨床試驗審批申請 |
公共服務(wù)事項 | 20.醫療器械說(shuō)明書(shū)更改告知申請 | 國家器審中心 |
21.醫療器械注冊/許可事項變更復審申請 |
22.創(chuàng )新醫療器械特別審查申請 |
公共服務(wù)事項 (暫緩開(kāi)通) | 23.醫療器械注冊證/變更文件補辦申請(暫緩開(kāi)通) | 器械注冊司 |
24.醫療器械注冊證/變更文件糾錯申請(暫緩開(kāi)通) | 受理和舉報中心/器審中心/器械注冊司 |
25.醫療器械注冊證/變更文件自行注銷(xiāo)申請(暫緩開(kāi)通) | 器械注冊司 |
26.自行撤回醫療器械注冊/注冊變更/延續注冊/復審申請(暫緩開(kāi)通) | 器審中心/器械注冊司 |
26.自行撤回醫療器械注冊/注冊變更/延續注冊/復審申請(暫緩開(kāi)通) | 器械注冊司 |
Q2:2019年6月24日之前受理的資料怎么辦����?
A:在此前受理的資料按照舊版的43��、44號文的要求執行����,該產(chǎn)品的延續注冊也可繼續按照43���、44號文的要求遞交紙質(zhì)資料�。在此之后受理的資料遞交就按照eRPS的要求執行���,其間過(guò)渡期可從線(xiàn)上申報或者線(xiàn)下申報兩種途徑擇其一�����。
Q3:過(guò)渡期的資料怎么辦�����?
A:過(guò)渡期可從線(xiàn)上申報或者線(xiàn)下申報兩種途徑擇其一�。線(xiàn)上eRPS提交不需紙質(zhì)材料����;線(xiàn)下遞交紙質(zhì)資料(含現場(chǎng)��、郵寄)還需再按照要求準備好相應U盤(pán)��,同時(shí)攜帶U盤(pán)�����、紙質(zhì)版資料以及紙質(zhì)版資料與電子版文檔一致性聲明至中心受理部門(mén)�����。
注意:
1.不可僅提交紙質(zhì)資料�����,紙質(zhì)資料無(wú)需復印多份���。
2.不可僅提交存有RPS ToC形式電子資料U盤(pán)����。
3.U盤(pán)電子資料一定要符合RPS ToC要求�����,確保文件夾結構正確���、RPS ToC要求必須提交的目錄項下文件正確�����、不可存有一個(gè)以上注冊申請項目�����、不可儲存有申報事項以外數據等�����。
4.自eRPS啟用后�,選擇線(xiàn)下途徑提交醫療器械注冊申請的�,建議盡量選擇現場(chǎng)辦理方式����,以方便申請人/注冊人與審評中心受理部門(mén)溝通交流�����。
Q4: 境外企業(yè)的公證性文件拆分掃描后是否還具有效應��?
A:境外公證性文件裝訂成冊公證�����,此前要求不可拆分���,拆分后無(wú)效應��。目前基于此部分資料需掃描后創(chuàng )建PDF文件����,允許拆開(kāi)掃描上傳也不影響其有效性����。
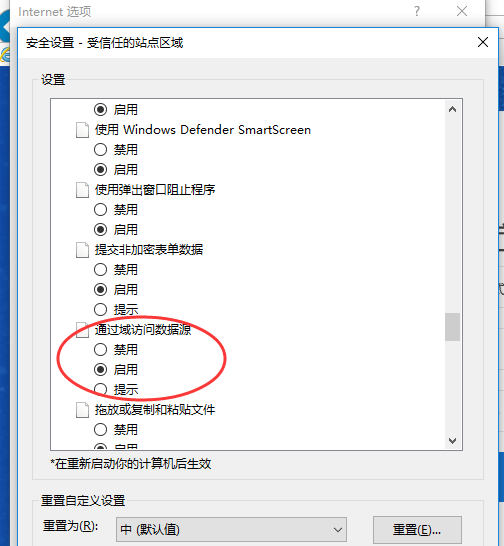
Q5:網(wǎng)頁(yè)版文件上傳長(cháng)時(shí)間出現上傳不成功怎么辦�?
A:工具→Internet選項→安全→自定義級別→啟用“通過(guò)域訪(fǎng)問(wèn)數據源”