醫療器械注冊質(zhì)量管理體系是什么��?是YY/T0287idtISO13485嗎�����?是醫療器械生產(chǎn)質(zhì)量管理規范嗎��?聽(tīng)過(guò)我講課的朋友們應該都清楚���,醫療器械注冊質(zhì)量管理體系是YY/T0287與ISO13485,及法規要求��、客戶(hù)要求�、產(chǎn)品特點(diǎn)和工藝特點(diǎn)等的融合��。今天�,從另一個(gè)視角���,為大家介紹有關(guān)醫療器械注冊體系核查的其它方面知識.
醫療器械注冊質(zhì)量管理體系是什么�����?是YY/T0287idtISO13485嗎����?是醫療器械生產(chǎn)質(zhì)量管理規范嗎����?聽(tīng)過(guò)我講課的朋友們應該都清楚��,醫療器械注冊質(zhì)量管理體系是YY/T0287與ISO13485,及法規要求����、客戶(hù)要求�、產(chǎn)品特點(diǎn)和工藝特點(diǎn)等的融合��。今天�,從另一個(gè)視角��,為大家介紹有關(guān)醫療器械注冊體系核查的其它方面知識.

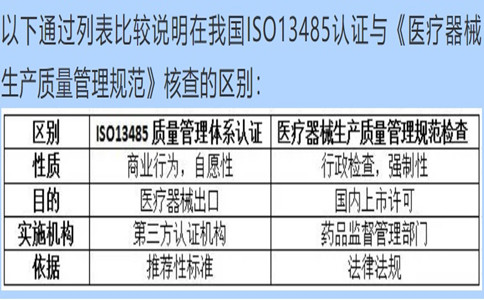
問(wèn):公司已經(jīng)通過(guò)了ISO13485的認證和年度評估����,辦理醫療器械生產(chǎn)許可時(shí)藥監局為什么還要來(lái)進(jìn)行生產(chǎn)質(zhì)量規范現場(chǎng)核查�����?
答:根據《醫療器械監督管理條例》規定����,第二類(lèi)����、第三類(lèi)醫療器械生產(chǎn)新開(kāi)辦��、變更和延續均為行政許可事項����,應當向所在地省����、自治區�、直轄市人民政府藥品監督管理部門(mén)申請生產(chǎn)許可�?�!夺t療器械生產(chǎn)質(zhì)量管理規范》及附錄是醫療器械生產(chǎn)企業(yè)必須執行的法規要求�,是獲得生產(chǎn)許可的基本條件��。
ISO13485標準在國內等同轉換為YY/T0287���,是醫療器械質(zhì)量管理體系推薦性行業(yè)標準�����,實(shí)施ISO13485認證的第三方認證機構不具備行政許可資格�����,通過(guò)第三方認證并不能作為上市許可的必要條件��。
問(wèn):質(zhì)量部門(mén)獨立行使權力在組織架構上應如何體現�����?有什么要求�?
答:按照《醫療器械生產(chǎn)質(zhì)量管理規范》的要求��,醫療器械生產(chǎn)企業(yè)應建立質(zhì)量管理部門(mén)�,獨立行使職能�����,對產(chǎn)品質(zhì)量的相關(guān)事宜負有決策的權利���。企業(yè)應成立專(zhuān)門(mén)的�、獨立的質(zhì)量管理部門(mén)并由最高管理者或其授權代表直接管轄�。質(zhì)量管理部門(mén)應包括QA及QC的職能����,具體職能應根據企業(yè)的實(shí)際情況在其職責文件中進(jìn)行明確規定��,例如質(zhì)量管理�、質(zhì)量控制���、質(zhì)量檢驗�����、產(chǎn)品放行���、讓步接收���、質(zhì)量審核���、質(zhì)量數據統計分析�、不合格品控制���、內部審核��、管理評審等����。產(chǎn)品上市放行應由質(zhì)量受權人負責���,質(zhì)量部門(mén)應對產(chǎn)品質(zhì)量具有絕對的���、獨立的決策權�,確保每批次原料�����、中間品��、終產(chǎn)品符合質(zhì)量要求���。
任何有關(guān)醫療器械注冊質(zhì)量管理體系疑問(wèn)��,歡迎您隨時(shí)方便與杭州證標客聯(lián)絡(luò )�。