江蘇省藥品監督管理局關(guān)于重新發(fā)布藥品��、醫療器械產(chǎn)品注冊費收費標準的公告
(2021年第5號)

根據國家有關(guān)最新規定和我省《省財政廳省物價(jià)局關(guān)于重新發(fā)布我省食品藥品監督管理部門(mén)行政事業(yè)性收費項目的通知》(蘇財綜〔2016]108號)���、《省發(fā)展改革委省財政廳關(guān)于降低藥品����、醫療器械產(chǎn)品注冊費收費標準的通知》(蘇發(fā)改收管發(fā)〔2019〕91號)要求���,現對目前執行的《江蘇省藥品監督管理局關(guān)于降低藥品��、醫療器械產(chǎn)品注冊費收費標準的公告》(蘇藥監財〔2019 7號)進(jìn)行修訂并重新發(fā)布���。修訂的主要事項如下:
一����、根據《藥品注冊管理辦法》(國家市場(chǎng)監督管理總局令第27號)第77��、79條�,省局辦理的藥品補充申請(含常規項���、需技術(shù)審評項)已改為備案事項�,據此�,停征藥品補充申請注冊費���。
二���、根據《關(guān)于繼續免征相關(guān)防疫藥品和醫療器械注冊費的公告》(財政部國家發(fā)展改革委公告2021年第9號)���,為支持疫情防控����,減輕企業(yè)負擔����,對進(jìn)入醫療器械應急審批程序并與新型冠狀病毒(2019-nCoV)相關(guān)的疫情防控產(chǎn)品���,免征醫療器械產(chǎn)品注冊費;對進(jìn)入藥品特別審批程序�、治療和預防新型冠狀病毒肺炎(COVID-19)的藥品�����,免征藥品注冊費�����。免征期限自2021年1月1日起至2021年12月31日止��。
三���、根據《市場(chǎng)監督管理行政許可程序暫行規定》(國家市場(chǎng)監督管理總局令第16號)�、《國家藥監局關(guān)于重新發(fā)布藥品注冊收費標準的公告》(2020年第75號)���,藥品�、醫療器械產(chǎn)品注冊申請人應當在收到《藥品注冊審批繳費通知書(shū)》�����、《醫療器械注冊審批繳費通知書(shū)》后15個(gè)工作日內按照要求繳納注冊費或提交減免申請����,未按要求繳納或提交減免申請的�,其注冊程序自行終止����。
四�����、將注冊申請人申報小微企業(yè)收費優(yōu)惠政策需提交的資料修訂為“上一年度企業(yè)所得稅納稅申報表((須經(jīng)稅務(wù)部門(mén)蓋章確認)或上一年度有效統計表(統計部門(mén)出具);新開(kāi)辦企業(yè)�,如無(wú)上述資料����,可提供上一個(gè)月的單位社會(huì )保險參保繳納證明(社會(huì )保險部門(mén)出具)”����。
以往規定與本公告不一致的��,以本公告為準��。本公告自發(fā)布之日起30日施行��。
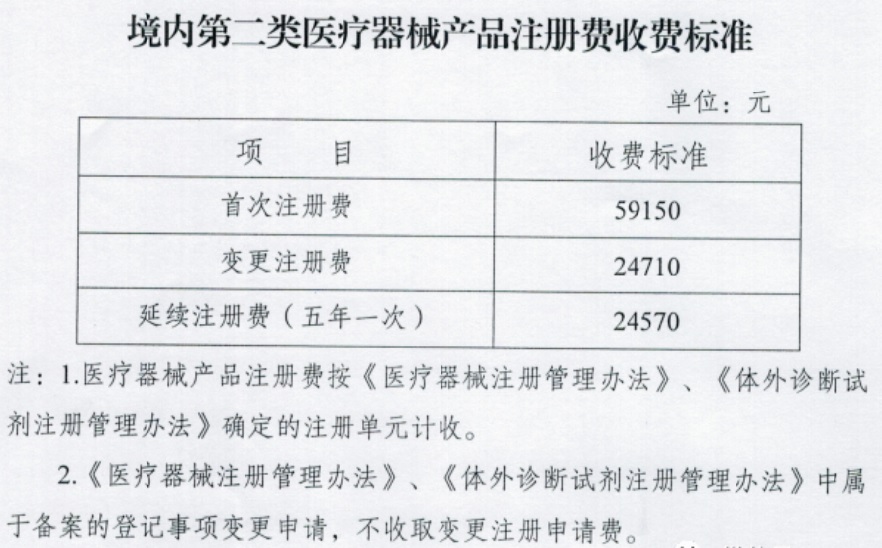
附件∶江蘇省第二類(lèi)醫療器械產(chǎn)品注冊費收費標準